Potencial de ação neural
A estimulação elétrica produzida pelos aparelhos de eletroterapia não invasiva irá estimular fibras neurais e musculares. Neste texto, iremos abordar somente os efeitos da estimulação elétrica nas fibras neurais.
O mecanismo de atuação pode ser resumido da seguinte forma:
O eletrodo negativo irá injetar cargas elétricas no exterior da membrana da fibra neural [3]. Se o estímulo elétrico apresentar intensidade suficiente para reduzir o potencial de membrana até -60mV, os canais de sódio dependentes de voltagem irão se abrir, permitindo a entrada de íons de sódio na célula. A entrada de íons de sódio irá disparar o potencial de ação, o qual será transmitido ao longo de toda a membrana e, em seguida, de uma célula a outra.
Por outro lado, o eletrodo positivo irá reduzir cargas no exterior da membrana, aumentando ainda mais o potencial de membrana e diminuindo a excitabilidade da fibra neural [3].
Para compreender melhor todo este processo, vamos explorar um pouco da fisiologia da membrana celular, do potencial de membrana e do potencial de ação.
Estrutura da membrana celular
A membrana celular é um marco na evolução da vida. Os primeiros organismos unicelulares só foram possíveis, porque as biomoléculas se organizaram de tal forma que possibilitaram o isolamento de moléculas e substâncias químicas em relação ao meio circundante. Esse isolamento foi feito pela membrana celular. A rigor, qualquer membrana (seja ela celular, nuclear ou de organela) tem a função de definir limites [1].
Quais são as biomoléculas envolvidas na formação da membrana celular e como elas se organizam?
Uma dessas biomoléculas são os lipídeos. Os lipídeos são popularmente chamados de “gorduras”. São uma classe heterogênea de compostos orgânicos, mas que têm em comum o fato de serem insolúveis em água. A membrana celular apresenta dois tipos de lipídeos mais importantes: os fosfolipídeos e o colesterol [1].
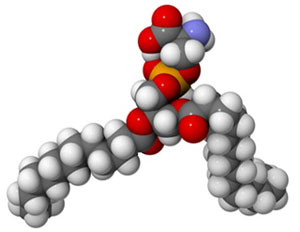
Fosfolipídeos são moléculas de lipídeos com fosfato. O fosfato é um radical de fósforo com oxigênio (PO4-3). O fosfato forma a cabeça e o lipídeo forma as caudas da molécula de fosfolipídeo. A figura a seguir mostra um fosfolipídeo típico da membrana celular: a fosfatidilserina.
Devido às suas propriedades químicas, os lipídeos não conseguem se dissolver em água. Então, quando qualquer lipídeo está imerso em água, as suas moléculas tendem a se agrupar, formando esferas. É exatamente isso que ocorre quando os fosfolipídeos estão imersos em meio aquoso, mas com uma propriedade especial:
Quando moléculas de fosfolipídeos estão em meio aquoso, as caudas lipídicas são repelidas pela água, mas são atraídas entre si. Isso faz com que as caudas lipídicas tendam a se agrupar frente a frente e lado a lado, formando duas fileiras. As porções fosfato sempre se posicionam em contato com o meio aquoso, enquanto as porções lipídicas sempre se posicionam internamente [1].
Na figura abaixo, há três formas de organização de lipídeos em meio aquoso:
- À esquerda, uma micela. Um aglomerado formado por apenas uma camada de moléculas lipídicas.
- No centro, um lipossoma. Um aglomerado formado por duas camadas de moléculas lipídicas.
- À direita, uma bicamada. Um aglomerado formado por duas camadas de moléculas lipídicas.
Em meio aquoso, os fosfolipídeos se organizam em duas camadas. É por isso que se diz que a membrana celular é uma bicamada. Os fosfolipídeos que formam a bicamada não são todos iguais. Há certa variação entre os tipos de fosfolipídeos, porque isso confere mais estabilidade à membrana.
Além dos fosfolipídeos, o colesterol também é um lipídeo importante na membrana celular. O colesterol faz com que a bicamada lipídica se torne ainda mais impermeável à água e auxilia na regulação da fluidez da membrana [1].
Tendo em vista que os lipídeos não são solúveis em água, a bicamada lipídica funciona como uma barreira que impede o livre trânsito de água e de substâncias solúveis em água para dentro e para fora da célula. É assim que o meio intracelular é isolado do meio circundante. Por outro lado, substâncias como oxigênio e dióxido de carbono facilmente atravessam a bicamada, por serem solúveis nesse meio e porque a bicamada é fluida e não sólida [1]. Sim, a bicamada lipídica não é uma parede totalmente sólida que impede todo e qualquer trânsito de substâncias. As moléculas lipídicas podem se mover na bicamada, abrindo espaços intermoleculares e permitindo a passagem de substâncias solúveis em meio lipídico.
Mas também é necessário que a célula receba água e substâncias solúveis em água (como íons). É aí que entra outra classe de biomoléculas: as proteínas. Proteínas são sequências de aminoácidos. Aminoácidos, por sua vez, são compostos orgânicos que sempre apresentam um átomo central de carbono, um grupo amina (H2N) e um grupo carboxila (COOH).
Na membrana celular, as proteínas geralmente estão ligadas à glicose, um carboidrato de fórmula C6H12O6. Portanto, são glicoproteínas. As glicoproteínas atravessam a bicamada lipídica, promovendo comunicação entre o meio intra e extracelular [1].
Na membrana celular, as proteínas formam canais que permitem a passagem de compostos solúveis em água [1]. Os canais proteicos são seletivos para certas moléculas ou íons devido às suas características estruturais: diâmetro, formato e carga elétrica [2]. Por exemplo, os canais de sódio apresentam diâmetro capaz de acomodar os íons sódio (Na+) e são carregados negativamente. Por outro lado, os canais de potássio apresentam diâmetro capaz de acomodar íons potássio (K+) e não são carregados.
Veja a seguir um desenho da membrana celular como um todo. A bicamada lipídica é atravessada por proteínas.
Para outras informações, veja os slides da aula de “Biomembranas” da Profª Ana Paula Araújo (IFSC-USP).
Potencial elétrico da membrana celular
A estrutura física da membrana celular não define apenas os limites da célula. Também define o potencial elétrico em torno dela. A membrana celular não é igualmente permeável a todos os íons. Se ela fosse, haveria a mesma quantidade de íons de cada um dos lados da membrana. Neste caso, haveria neutralidade elétrica. Como a membrana não é igualmente permeável a todos os íons, há desequilíbrio na concentração de íons de cada lado da membrana, o que gera diferenças de potencial elétrico.
Íon é qualquer partícula eletrizada que não está se neutralizando: se o íon for positivo (cátion), significa que ele perdeu elétrons e se o íon for negativo (ânion), significa que ele ganhou elétrons. Existem canais proteicos específicos para cada íon. Assim, se íons de sódio e de potássio conseguem ultrapassar a membrana celular, é porque há canais proteicos específicos para esses íons. Caso contrário, eles não conseguiriam se difundir para dentro e para fora da célula.
Além disso, há outros fatores que influenciam o grau de permeabilidade da membrana a um determinado íon [2]:
- O número de canais proteicos para aquele íon: quanto maior o número de canais, maior a permeabilidade.
- A solubilidade do íon em meio lipídico: quanto mais solúvel, mais permeável.
- O peso molecular do íon: quanto menor o peso molecular, mais permeável.
- A espessura da membrana: quanto menor a espessura, maior a permeabilidade.
- A temperatura: quanto maior a temperatura, maior a permeabilidade.
Durante o repouso, devido às diferenças de permeabilidade, há concentrações iônicas diferentes nos dois lados da membrana. No lado interno, há maior concentração de íons potássio, magnésio e fosfato. No lado externo, há maior concentração de íons sódio, cálcio e cloreto. São exatamente essas diferenças de concentrações de íons que geram a diferença de potencial elétrico na membrana [3].
Nas células neurais e musculares, três fatores são os mais importantes para o estabelecimento da diferença de potencial elétrico da membrana: o potencial de difusão de potássio, o potencial de difusão de sódio e a bomba de sódio e potássio.
Os íons de potássio (K+) tendem a se concentrar no interior da membrana. Há 35 vezes mais íons potássio no lado interno em relação ao externo da membrana, gerando um potencial de -94mV [3]. O potencial é negativo, porque é sempre medido em relação ao lado externo da membrana.
Por outro lado, os íons de sódio (Na+) tendem a se concentrar no exterior da membrana. Há 10 vezes mais íons sódio no lado externo em relação ao interno da membrana, gerando um potencial de +61mV [3].
Os íons potássio são mais importantes para o estabelecimento do potencial elétrico da membrana do que os íons sódio, porque a membrana é 100 vezes mais permeável ao potássio do que ao sódio durante o repouso [3].
Além disso, a bomba de sódio e potássio transporta íons de um lado para outro da membrana. A bomba de sódio e potássio é um processo ativo, que necessita de energia para seu funcionamento. Tendo em vista que a bomba transporta três íons de sódio para fora e dois íons de potássio para dentro da célula, ela também gera diferença de potencial elétrico, algo em torno de -4mV [3]. Veja aqui um esquema da bomba de sódio e potássio da membrana celular.
A interação entre os potenciais de difusão do potássio, do sódio e da bomba de sódio e potássio gera uma diferença de potencial elétrico na membrana das fibras neurais de -70mV durante o repouso [3]. Veja aqui um desenho esquemático desse potencial.
A bomba de sódio e potássio é um mecanismo extremamente importante, porque também controla o volume celular, impedindo que a célula rompa por excesso de água [2]. No citoplasma, há grande concentração de proteínas, que são moléculas grandes e que não conseguem atravessar a membrana em direção ao meio extracelular. Devido à alta concentração de proteínas, a tendência é que moléculas de água entrem na célula para diluir o fluido intracelular. Se a osmose de água ocorresse livremente pelos canais proteicos, a célula iria dilatar até romper. Entretanto, quando a célula começa a dilatar, a bomba de sódio e potássio é ativada. A transferência de três íons para o meio externo e de apenas dois para o meio interno, faz com que o movimento de osmose de água se inverta, reequilibrando o volume celular.
Potencial de ação
O potencial elétrico da membrana permanece em -70mV quando a célula está em repouso, ou seja, quando não é estimulada. Que fatores são capazes de modificar o potencial de membrana, estimulando a célula? Fatores mecânicos, químicos ou elétricos [3]. São todos mecanismos utilizados pelo organismo. Por exemplo: pressões mecânicas sobre a pele terminarão por excitar nervos sensoriais; neurotransmissores transmitirão impulsos de um neurônio a outro; estímulos elétricos transmitirão impulsos de uma célula muscular a outra. Todos esses estímulos podem desequilibrar o potencial de membrana e disparar o potencial de ação.
Durante o repouso, as cargas elétricas ficam ordenadas ao longo da membrana. As cargas positivas ficam no lado externo e as negativas, no lado interno. Devido à carga negativa (-70mV), a membrana está polarizada [3].
Se o número de íons sódio que entram na célula for maior do que o número de íons potássio que saem da célula, a polarização no interior da célula começar a diminuir. Se a redução na polarização atingir -60mV, abrem-se as portas de ativação dos canais de sódio dependentes de voltagem, permitindo que íons sódio entrem na célula. Conforme mais canais de sódio dependentes de voltagem vão se abrindo, mais íons sódio entram na célula e mais o potencial elétrico tende a zero, podendo chegar a +35mV. A membrana se torna 500 vezes mais permeável ao sódio do que no repouso. Tendo em vista que a carga negativa é perdida, a membrana está despolarizada [3].
A mesma despolarização que abre as portas de ativação, fecha as portas de inativação dos canais de sódio dependentes de voltagem. A diferença é que a porta de ativação abre rapidamente, enquanto a de inativação fecha lentamente. Quando a porta de inativação se fecha totalmente, a entrada de íons sódio fica bloqueada [3].
Os canais de potássio dependentes de voltagem também tem um papel na geração do potencial de ação, mas muito menos importante do que os canais de sódio dependentes de voltagem. Os canais de potássio dependentes de voltagem se abrem lentamente durante a despolarização, permitindo que íons potássio saiam da célula [3].
Veja aqui um desenho do processo de abertura e fechamento dos canais dependentes de voltagem .
Essas rápidas mudanças no potencial de membrana são chamadas de “potencial de ação”. Veja aqui um esquema de todo o processo.
Uma vez iniciado, o potencial de ação irá se propagar ao longo da membrana celular, porque a despolarização de um canal de sódio dependente de voltagem consegue despolarizar o próximo. A transmissão da despolarização ao longo da fibra nervosa ou muscular é chamada de impulso.
Após a ocorrência do potencial de ação e a transmissão do impulso, a bomba de sódio e potássio reestabelece o potencial de repouso da membrana em -70mV [3].
A descoberta dos canais de sódio e potássio e seu papel durante o potencial de ação rendeu a John Eccles, Alan Hodgkin e Andrew Huxley o Prêmio Nobel de Medicina em 1963.
Referências
[1] Guyton, A. C. & Hall, J. E. (1996). The cell and its function. In: Textbook of medical physiology (pp. 11-26). 9th ed. Philadelphia: W. B. Saunders Co.
[2] Guyton, A. C. & Hall, J. E. (1996). Transport of ions and molecules through the cell membrane. In: Textbook of medical physiology (pp. 43-55). 9th ed. Philadelphia: W. B. Saunders Co.
[3] Guyton, A. C. & Hall, J. E. (1996). Membrane potentials and action potentials. In: Textbook of medical physiology (pp. 57-72). 9th ed. Philadelphia: W. B. Saunders Co.